Publicado em 17/02/2022, às 16h45 - Atualizado às 17h14 por Redação Pais&Filhos
Nesta última quinta-feira, 17 de fevereiro, a Agência Nacional de Vigilância Sanitária (Anvisa) registrou o primeiro autoteste para Covid-19 no Brasil, o “Novel Coronavírus (Covid-19) Autoteste Antígeno”, da empresa CPMH Comércio e Indústria de Produtos Médicos-Hospitalares e Odontológicos.
“A publicação do registro está na Resolução RE 533/2022, publicada hoje no Diário Oficial da União. A disponibilidade do produto no mercado depende da empresa detentora do registro”, afirmou a Anvisa. De acordo com a Anvisa, o pedido foi avaliado por 16 dias.
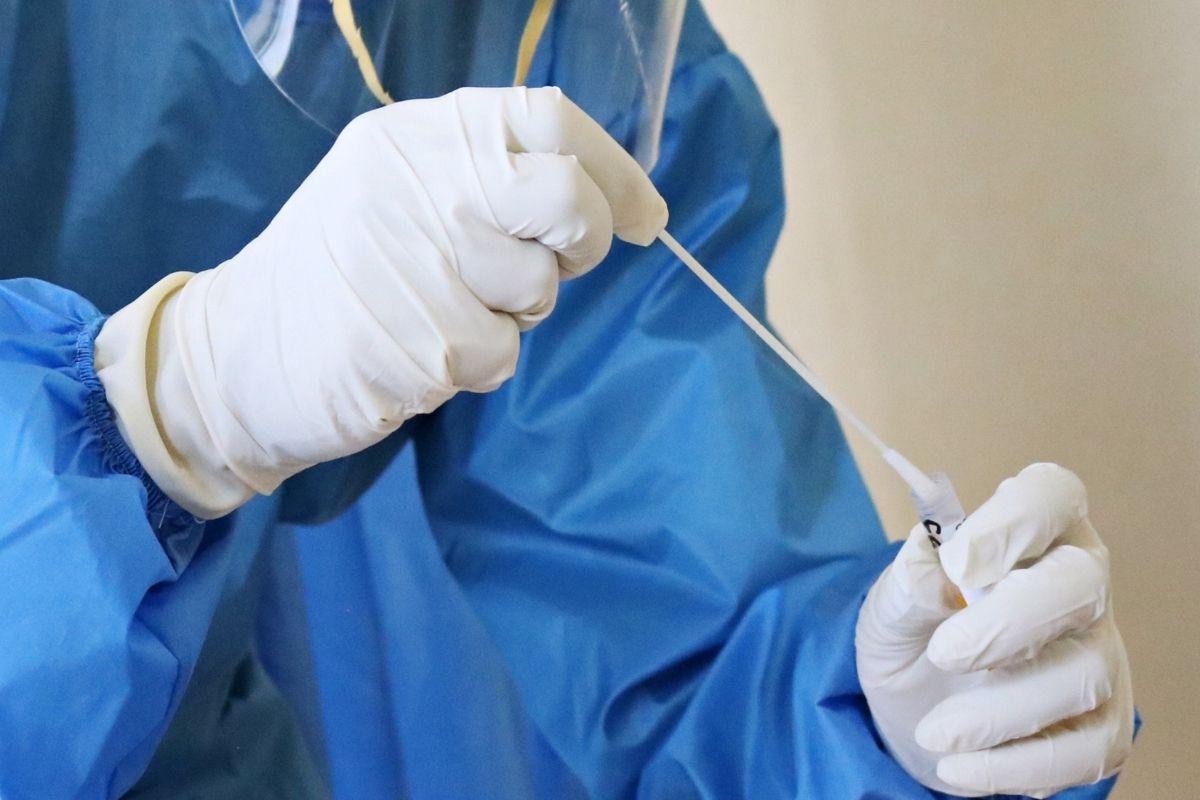
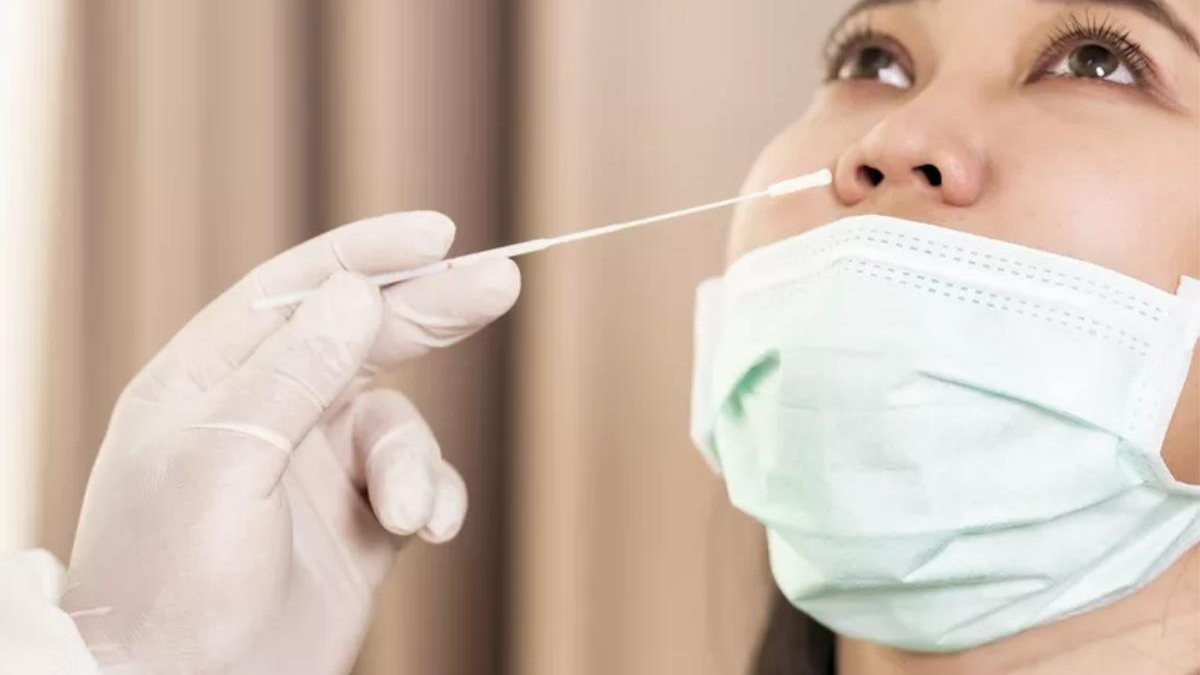
Lembrando que a medida vale apenas para os testes de antígenos, feitos a partir do swab que coleta o material no fundo da boca e do nariz e busca sinais de anticorpos gerados pelo corpo após a infecção, e não o RT-PCR que é mais preciso, mais demorado e que detecta a presença do material genético do coronavírus.
De acordo com os diretores da Anvisa, o Ministério da Saúde vai incluir orientações sobre o uso dos autotestes em uma atualização do “Plano Nacional de Expansão de Testagem para Covid-19” (PNE Teste). Além disso, sem impor como condição, a Anvisa espera que as empresas desenvolvam estratégias para que – voluntariamente – os compradores dos autotestes informem os resultados por meio de sistema na internet.

“A partir do resultado positivo, procure uma unidade de atendimento de saúde (ou teleatendimento) para que um profissional de saúde realize a confirmação do diagnóstico, notificação e orientações pertinentes”, afirmou a relatora Cristiane Rose Jourdan Gomes, citando o ministério da Saúde.
Leia também

Bebês
Nomes femininos raros: veja opções chiques e únicas para meninas

Família
Ticiane Pinheiro fala sobre gravidez e chegada de segundo filho com César Tralli

Bebês
Nasceu! Fernanda Paes Leme dá à luz primeira filha com Victor Sampaio

Família
Sabrina Sato se declara para Nicolas Prattes após Duda Nagle anunciar separação

Bebês
180 nomes femininos diferentes: ideias de A a Z para você chamar a sua filha

Família
Gêmeas siamesas falam sobre relações íntimas após uma assumir namoro

Gravidez
Isis Valverde posta foto grávida ao lado de amiga e faz declaração: "Alegria transborda"

Bebês
Nomes japoneses femininos: 304 opções lindas para você conhecer