Publicado em 11/11/2020, às 09h08 - Atualizado às 09h16 por Letícia Mutchnik, filha de Sofia e Christiano
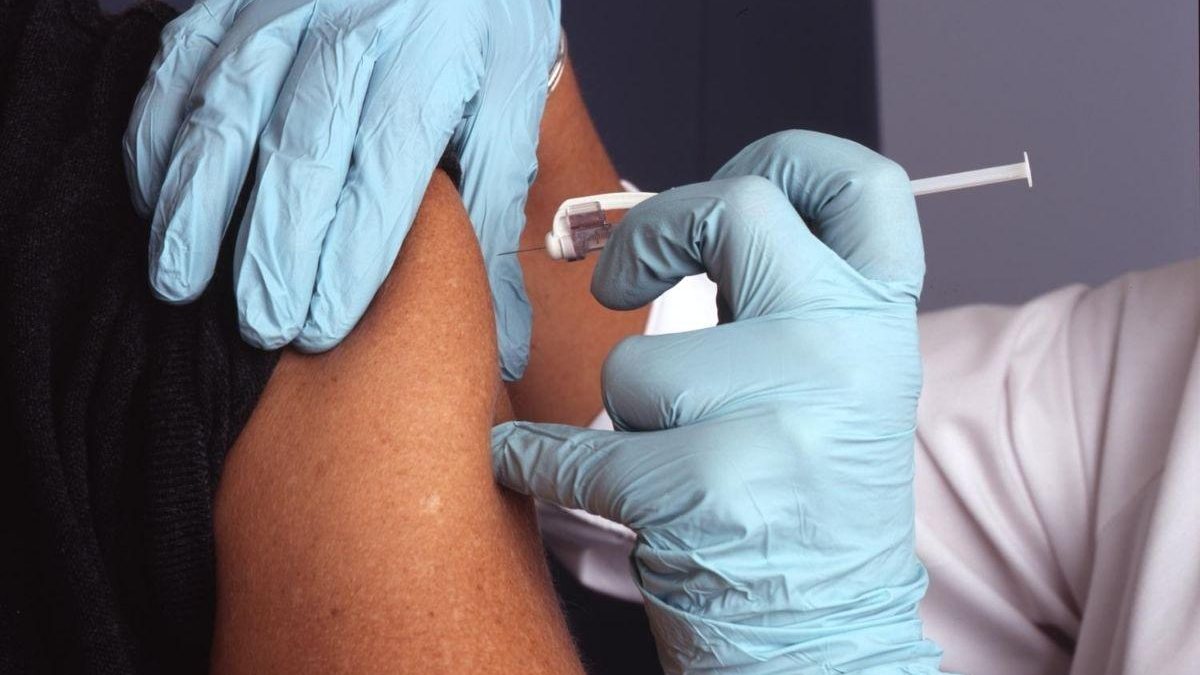
Nesta quarta-feira, 11 de novembro, a Agência Nacional de Vigilância Sanitária (Anvisa) autorizou a retomada de testes da vacina contra a Covid-19, a CoronaVac, que, segundo a CNN, tem sido desenvolvida pela chinesa Sinovac e pelo Instituto Butantan. Isso tudo após grande controvérsia na última terça-feira, 10 de novembro.
“Após avaliar os novos dados apresentados pelo patrocinador depois da suspensão do estudo, a ANVISA entende que tem subsídios suficientes para permitir a retomada da vacinação e segue acompanhando a investigação do desfecho do caso para que seja definida a possível relação de causalidade entre o EAG inesperado e a vacina”, informou a agência por meio de uma nota.
A Anvisa havia suspendido os estudos da vacina após ser informada de um “evento adverso grave” de um dos voluntários. Apesar dos dados serem sigilosos, de acordo com boletim de ocorrência obtido pelo G1, a causa de morte foi suicídio. Sendo assim, desconexo da segurança do imunizante.
Entenda mais
A Anvisa informou na noite da última segunda-feira, 9 de novembro, a suspensão temporária dos testes em humanos da CoronaVac. A interrupção foi feita por causa de um “evento adverso grave” que teria acontecido no último dia 29. A causa específica, no entanto, não foi anunciada.
A vacina era uma das principais candidatas a imunizante contra a Covid-19, principalmente no estado de São Paulo, que possui uma parceria com o laboratório chinês Sinovac Biotech para a fabricação e desenvolvimento do medicamento no Instituto Butantan. Com a suspensão, nenhum novo voluntário pode ser vacinado.

O Instituto Butantan já afirmou em nota que “foi surpreendido” pela ação da Anvisa e que está “apurando em detalhes o que houve com o andamento dos estudos clínicos da Coronavac”. Apesar da surpresa, a decisão está prevista nas normas da Agência e fazem parte dos chamados procedimentos de “Boas Práticas Clínicas”.
Estão entre os efeitos colaterais considerados “graves” na testagem de uma vacina:
- Morte
- Evento adverso potencialmente fatal
- Incapacidade ou invalidez persistente
- Internação hospitalar do paciente
- Anomalia congênita ou defeito de nascimento
- Qualquer suspeita de transmissão de agente infeccioso por meio de um dispositivo médico
- Evento clinicamente significante.
10º Seminário Internacional Pais&Filhos
O 10º Seminário Internacional Pais&Filhos – Quem Ama Cria está chegando! Ele vai acontecer no dia 1 de dezembro, com oito horas seguidas de live, em formato completamente online e grátis. E tem mais: você pode participar do sorteio e ganhar prêmios incríveis. Para se inscrever para os sorteios, ver a programação completa e assistir ao Seminário no dia, cliqueaqui!
Leia também

Bebês
Fernanda Paes Leme recusa visitas após o nascimento da filha: "Não consigo e não quero"

Bebês
Nomes femininos raros: veja opções chiques e únicas para meninas

Família
Causa da morte de jovem após encontro com jogador do Corinthians vem à tona 2 meses depois

Bebês
180 nomes femininos diferentes: ideias de A a Z para você chamar a sua filha

Gravidez
Suposta mãe do 3º filho de Neymar confirma gravidez nas redes sociais

Família
Alok compartilha vídeo em família para anunciar: "Agora somos 6"
Gravidez
Sintomas de gravidez: nos primeiros dias, que ninguém sabe, de menino e menina e muito mais

Família
Graciele Lacerda fala sobre chegada de filho com Zezé di Camargo