Publicado em 03/06/2022, às 15h17 - Atualizado às 15h50 por Carolina Ildefonso, mãe de Victor
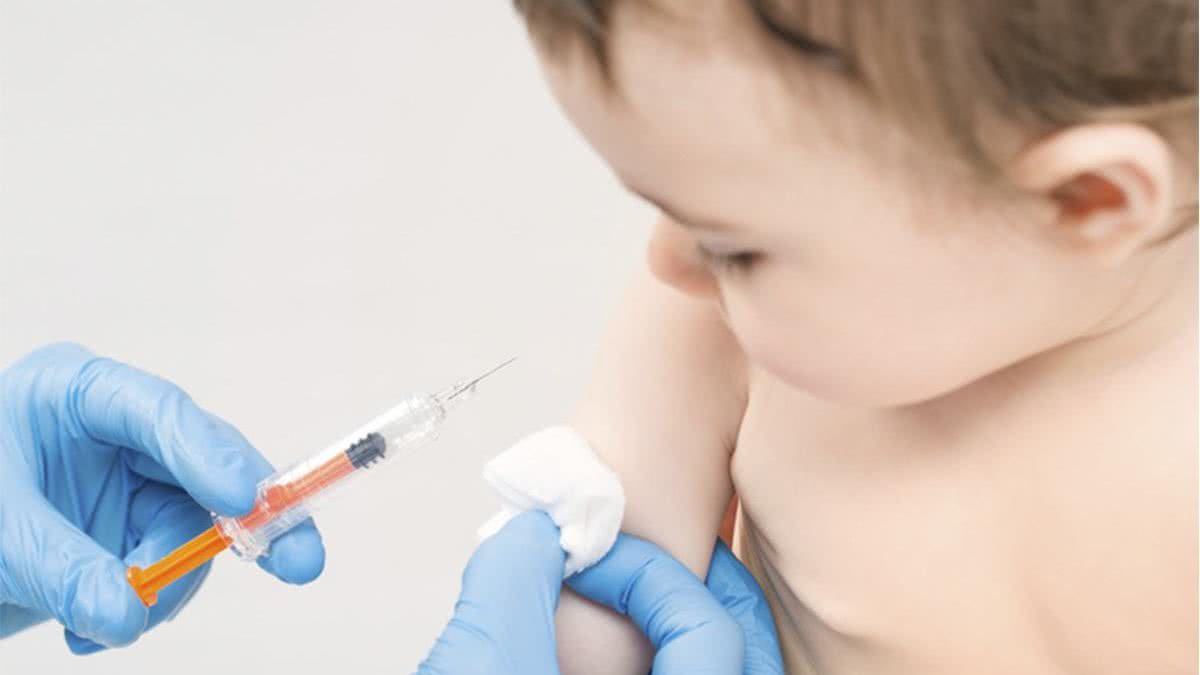
Com a pandemia da covid-19, temos visto cada vez mais os benefícios da vacinação. Por mais que o vírus ainda esteja em circulação, os sintomas da doença ficaram mais leves e as mortes diminuíram drasticamente.
Mas para os pais, a tranquilidade ainda não está completa, pois ainda não há vacina contra a covid-19 aqui no Brasil, autorizada pela Agência Nacional de Vigilância Sanitária, para menores de cinco anos. Isso porque o desenvolvimento de um imunizante segue diversos processos e padrões para atestar a qualidade até a aprovação dos órgãos reguladores.
Mas esse momento tão esperado está prestes a acontecer. Um novo estudo pediátrico da vacina contra a covid-19, realizado pelo Centro Paulista de Investigação Clínica – Cepic está em andamento, em São Paulo, e busca crianças que possam ser voluntárias, dessa vez com o imunizante da Pfizer Biontech.
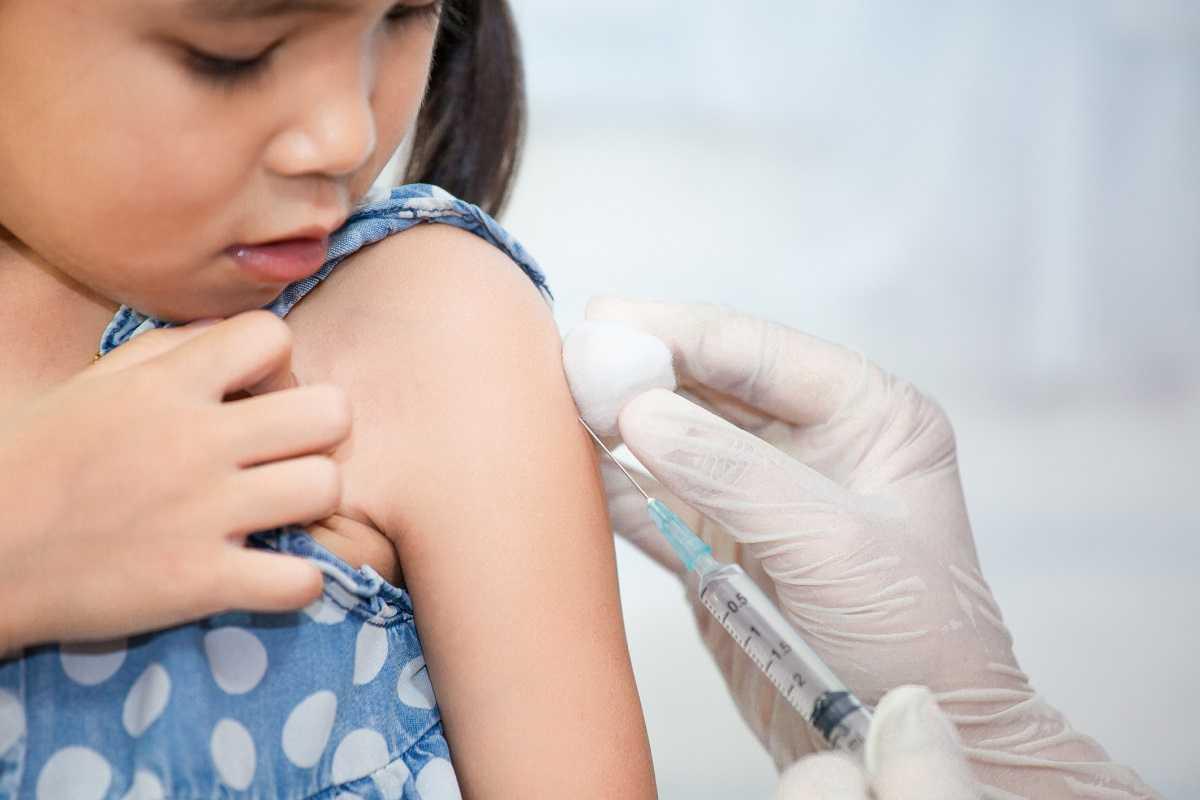
Segundo o diretor do Cepic e coordenador da pesquisa, Cristiano Zerbini, o estudo tem tido bons resultados em outros lugares no mundo. Nos Estados Unidos, por exemplo, a Pfizer concluiu a solicitação de autorização de uso emergencial junto à Food and Drug Administration (FDA). “O objetivo da pesquisa é descobrir se essa vacina pode produzir uma resposta imunológica contra a covid-19 e se é segura quando aplicada em crianças de seis meses a quatro anos de idade”, define Cristiano.
Conforme os resultados preliminares das fases 2 e 3 do estudo realizado nos EUA, foi constatado um índice de 80,3% de eficácia para essa faixa etária. Após a aplicação da terceira dose foram identificados apenas 10 casos sintomáticos, entre os 1678 voluntários.
Como será a aplicação das doses da Pfizer
Cristiano explica que as doses não serão as mesmas aplicadas em adultos e que serão dividas em três etapas. Da primeira para a segunda dose terá um espaçamento de 21 dias, já a terceira dose só será aplicada de 4 a 6 meses após a segunda. Como parte dos procedimentos, um terço dos participantes receberá placebo e o restante o imunizante, de fato. Mas todos serão acompanhados periodicamente por uma equipe multidisciplinar.
Cristiano reforça ainda que participar de um estudo clínico é uma decisão pessoal e muito importante não só para a proteção da família, como de toda a população.
As famílias interessadas devem entrar em contato com a equipe do Centro Paulista de Investigação Clínica para receber todas as informações necessárias e agendar o dia e horário, por meio dos telefones (11) 2271-3456 ou (11) 97414-0298, ou do e-mail [email protected].
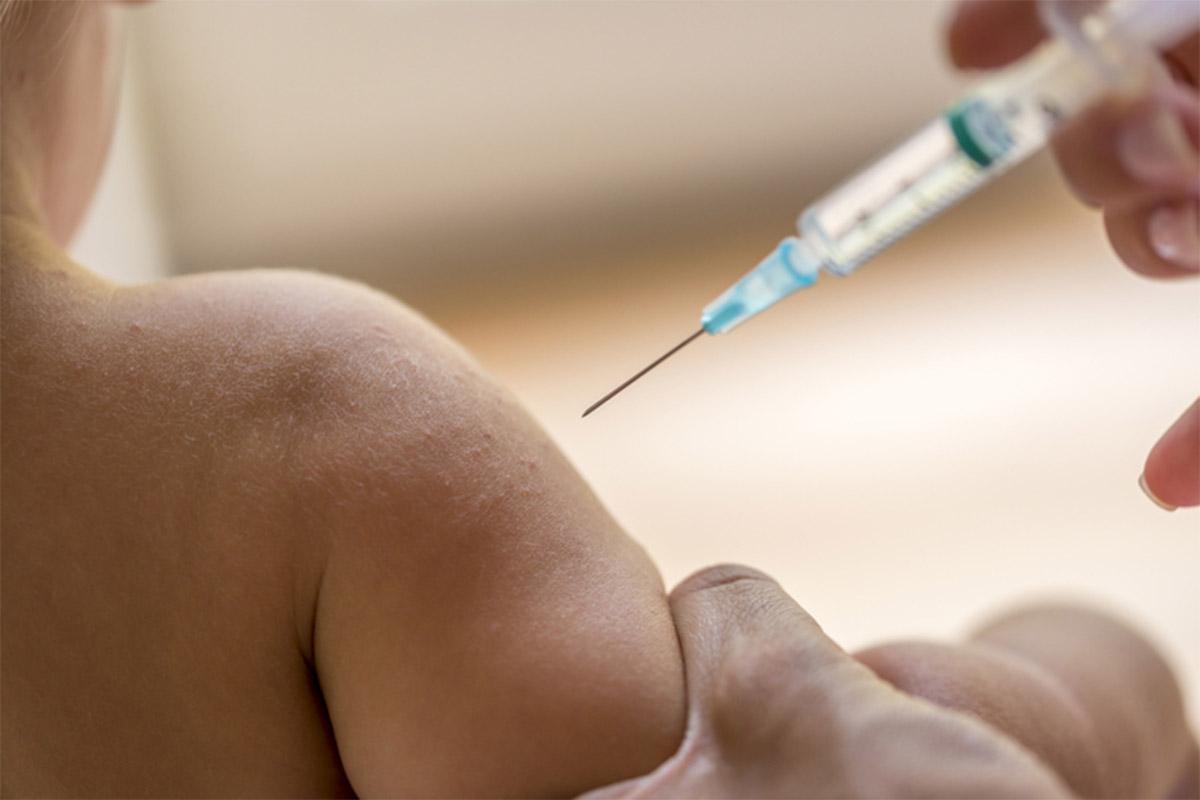
Coronavac em crianças
Desde 20 de janeiro, a Coronavac já é aplicada em crianças a partir de 6 anos de idade. Mas para os menores, esse imunizante também não está liberado. Essa semana, o Butantan enviou uma nova remessa de documentos que estavam pendentes, incluindo resultados do estudo realizado no Chile para autorizar a aplicação em crianças de 3 a 5 anos, porém a análise ainda não foi concluída.
Em nota, a agência reguladora informou que vai iniciar a análise técnica e avaliar a necessidade de nova discussão com as sociedades médicas. Mas ressaltou que mantém o seu compromisso na avaliação das vacinas, fundamentando as suas ações na legalidade e nos parâmetros estabelecidos em suas normas, convergentes com as principais autoridades estrangeiras e com os princípios científicos.
Leia também

Família
Causa da morte de jovem após encontro com jogador do Corinthians vem à tona 2 meses depois

Bebês
Fernanda Paes Leme recusa visitas após o nascimento da filha: "Não consigo e não quero"

Bebês
Nomes femininos raros: veja opções chiques e únicas para meninas

Bebês
180 nomes femininos diferentes: ideias de A a Z para você chamar a sua filha

Gravidez
Suposta mãe do 3º filho de Neymar confirma gravidez nas redes sociais
Gravidez
Sintomas de gravidez: nos primeiros dias, que ninguém sabe, de menino e menina e muito mais

Família
Alok compartilha vídeo em família para anunciar: "Agora somos 6"

Família
Davi explica detalhes do fim de relacionamento com Mani: "Fiquei em estado de choque"