Publicado em 14/12/2020, às 16h37 - Atualizado às 16h37 por Maria Laura Saraiva, Filha de Laise e Carlos
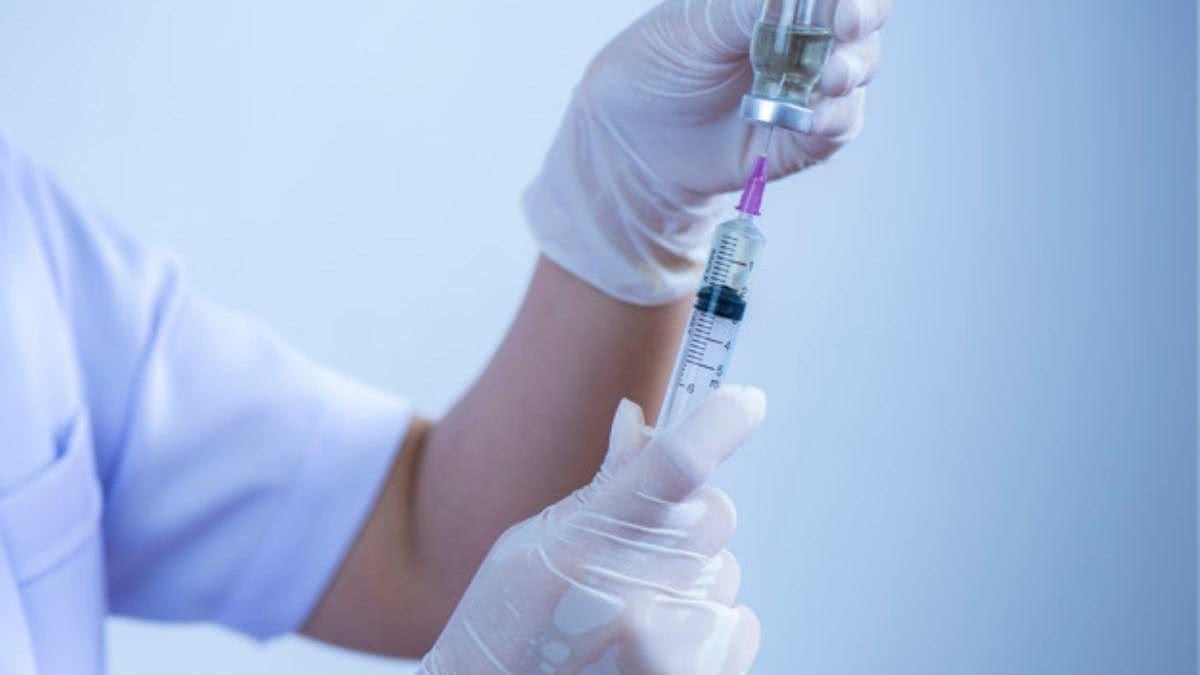
A Agência Nacional de Vigilância Sanitária (Anvisa) informou nesta segunda-feira, 14 de dezembro, que avaliará o pedido de uso emergencial das vacinas contra a Covid-19 em até dez dias depois da solicitação. O anúncio foi divulgado no mesmo dia em que o Governo de São Paulo informou que desistiu de apresentar o requerimento de uso emergencialnesta terça-feira.
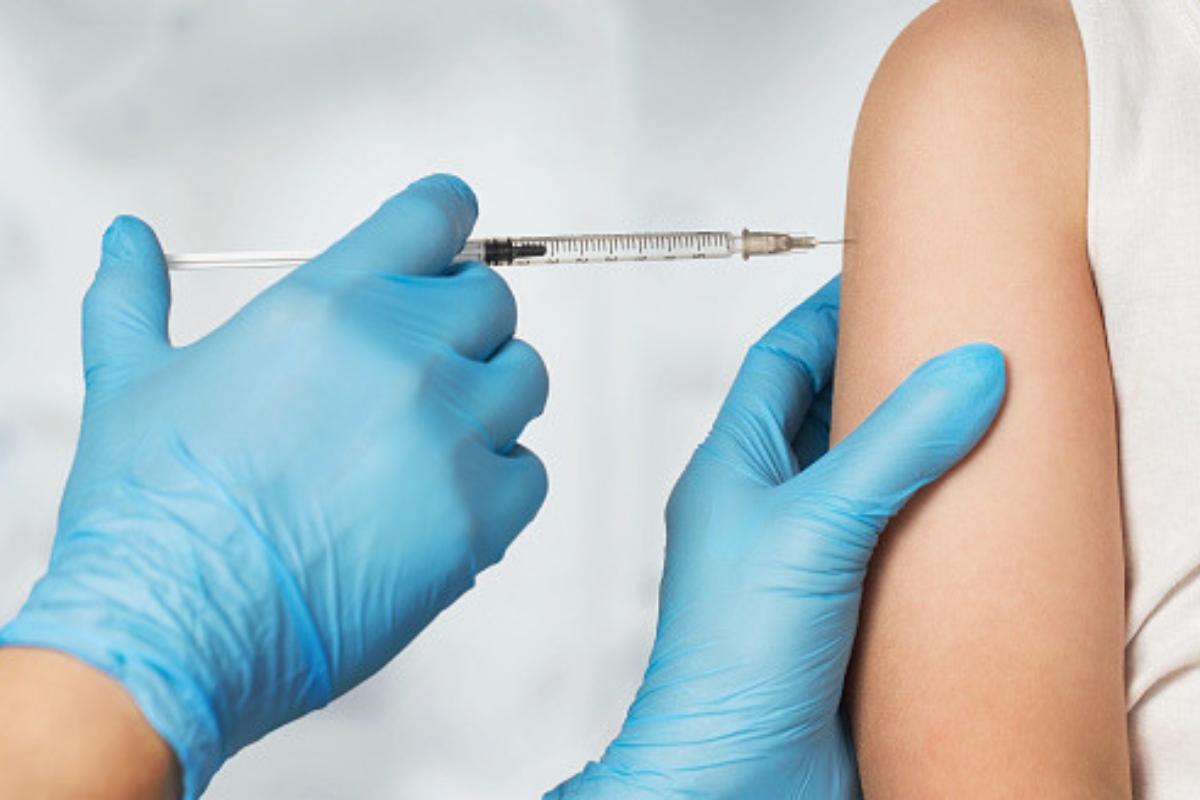
“Se todo os documentos necessários tiverem sido submetidos à Anvisa pelos fabricantes da vacina, a Anvisa estima que o prazo de até 10 (dez) dias para concluir a avaliação quanto à autorização de uso emergencial, desde que sejam vacinas das empresas que venham apresentando dados para Anvisa e possuem ensaios clínicos em condução no Brasil”, informou a agência.
O prazo estipulado pela Anvisa nesta segunda-feira não tem relação com a chamada Lei Covid, que prevê e 72 horas para a manifestação da agência caso uma das vacinas seja registrada nos órgãos internacionais de referência. Assim como não apresenta ligação com os 60 dias para a análise de pedidos de registro definitivo.
A Anvisa confirmou que ainda não recebeu pedidos oficiais do uso emergencial e que “está trabalhando em tempo integral”, organização que deve ser mantida nas semanas de Natal e Ano Novo.
Leia também

Família
Anderson Leonardo, do Molejo, morre aos 51 anos de câncer

Família
Ex-namorada de Anderson, do Molejo, fala sobre morte do cantor: "Arrasada"

Bebês
Bebê de 1 ano come fast food todos os dias e bebe seis latas de Coca-Cola: "É difícil dizer não"

Bebês
180 nomes femininos diferentes: ideias de A a Z para você chamar a sua filha
Gravidez
Sintomas de gravidez: nos primeiros dias, que ninguém sabe, de menino e menina e muito mais

Bebês
Nomes americanos femininos: mais de 1000 opções diferentes para você se inspirar

Família
Mãe diz que se arrependeu de adotar filha após conseguir engravidar: "Nunca senti que ela era minha"

Bebês
Nomes bíblicos femininos: veja a lista com opções lindas e fortes para meninas