
Publicado em 10/12/2020, às 10h08 - Atualizado às 10h29 por Cinthia Jardim, filha de Luzinete e Marco
Nesta quinta-feira, 10 de dezembro, durante uma coletiva de imprensa no início da tarde, o governador do Estado de São Paulo, João Doria, anunciou que o Instituto Butantan deu início à produção da CoronaVac, vacina contra o novo coronavírus.

O governador explicou ainda que mais funcionários foram contratados para dar início a produção. “Com isso, a capacidade de produção da vacinachegará a 1 milhão de doses por dia”, explica. Atualmente, 11 estados já formalizaram o pedido para o envio da CoronaVac a outros lugares do país. “São Paulo vai ajudar todos os estados brasileiros, assim como os municípios, para juntos salvarmos vidas.

Sobre o trabalho de produção, Dimas Covas, diretor do Instituto Butantan, explicou que a fábrica possui 1.880 m² de área produtiva e que já contava com uma equipe de 245 colaboradores. Para a produção da CoronaVac, serão contratados mais 120. A linha operará 24 horas por dia, nos sete dias da semana. “A primeira vacina no Brasil já está pré-disponível para a vacinação. É fruto de todas os nossos esforços e batalhas”, comenta. “Nós estamos muito orgulhosos de anunciar a produção desta vacina aqui no Instituto Butatan”, concluiu.
Plano de vacinação
Na segunda-feira, 7 de dezembro, o Governo de São Paulo anunciou como será o plano de vacinação da CoronaVac. Feita pelo laboratório chinês Sinovac, em parceria com o Instituto Butantan, há a previsão de que a população possa receber as primeiras doses em janeiro de 2021.
Na terceira fase de testes, a vacina precisa ainda ter a eficácia comprovada para, em seguida, ser liberada pela Agência Nacional de Vigilância Sanitária (Anvisa). O governo estadual disse ainda na última semana que o relatório final de testes será enviado em dezembro, e que não será necessário o uso emergencial da vacinaneste período.
Em uma campanha similar a de vacinação para gripe, José Medina, coordenador do Centro de Contingência para Covid-19, informou que a imunizaçãodeve começar com profissionais de saúde e pessoas acima dos 60 anos. “Quem tem entre 60 anos, a letalidade é de 3%. E ela é gradativamente subindo quem tem mais de 80 anos, até 80, 89 é de 32% e mais de 90 anos, é de 39%. E esse é o principal critério para a utilização da vacinação. Talvez o principal critério a ser utilizado é a vacinação das pessoas acima de 60 anos. São as pessoas quem têm mais risco, são as pessoas que saturam o sistema de saúde. Além disso, a vacinação dessas pessoas quebra o círculo de circulação do vírus”, explicou.
Sobre o plano de imunização geral, até o momento, o Governo Federal não divulgou o planejamento definitivo de vacinação e ainda não possui a licitação para continuar o atendimento. O prazo mínimo é de 60 a 90 dias para atender após aprovação.
Como irá funcionar
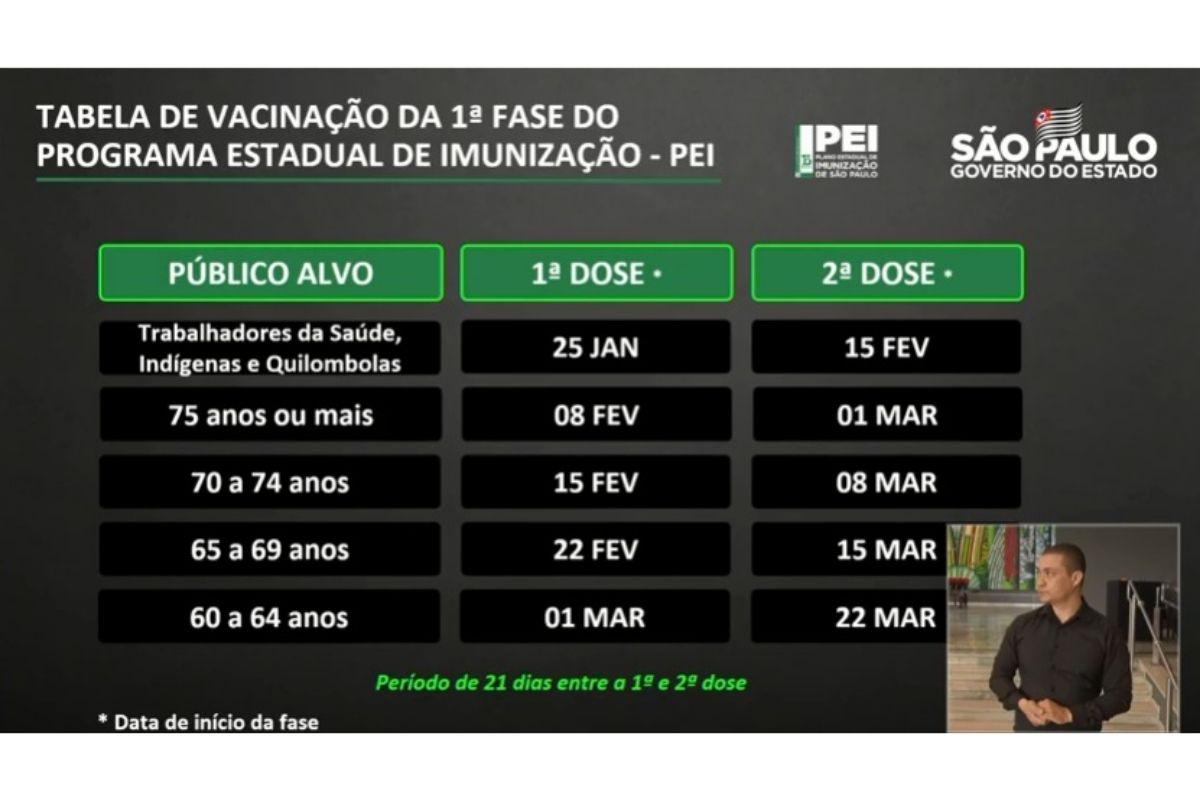
A partir do dia 25 de janeiro, João Doria explicou que será iniciado o plano estadual de vacinação. “As vacinas devem ser aplicadas imediatamente na população brasileira. Cada vida importa, e importa muito”, reforçou o governador. Para a primeira fase, será priorizado a imunização dos profissionais de saúde e pessoas acima de 60 anos. Para este segundo grupo, a consideração da escolha foi pela incidência de óbitos, que ocorreu 70% em pacientes acima desta faixa etária.

Com o objetivo de imunizar também os profissionais de saúde de outros estados, serão disponibilizadas 4 milhões de doses, que devem ser solicitadas com antecedência para serem entregues a partir de 25 de janeiro. No estado de São Paulo, os postos de atendimento à saúde serão ampliados para 10 mil. Para que todo o sistema funcione bem, serão implementadas estratégias em farmácias, escolas, quartéis, terminais de ônibus e ainda via drive thru. “A campanha contará com logística e segurança”, comenta Doria.
Os horários de funcionamento dos postos serão de segunda a sexta, das 7h às 22h*, e aos sábados, domingos e feriados, das 7h às 17h* (podendo ser estendido, se necessário, até as 22h). “Nós temos agulhas e seringas necessárias para vacinar este público. Já disponibilizamos todo o estoque”, garante Jean Gorinchteyn, Secretário de Saúde de São Paulo.
Durante a campanha de imunização, antecipada para janeiro no plano estadual, cada cidadão receberá duas doses da vacina, devendo ter um período de 21 dias entre elas. Para idosos, é pedido preferencialmente que os postos de saúde sejam procurados pela parte da manhã, com o intuito de evitar aglomerações. “O retorno a normalidade só ocorrerá com a vacinação“, completa o Secretário de Saúde de São Paulo.
De acordo com os estudos realizados durante a fase 1 e 2 com mais de 50 mil voluntários, 94,7% não tiveram nenhum evento adverso. Dos que apresentaram alguma, 99,7% foram dor no local e dor de cabeça. Segunda dados da revista científica The Lancet, a CoronaVac é uma das mais prestigiadas vacinas do mundo, tendo resposta imune em 97% dos casos.
Autorização temporária emergencial
A Anvisa decidiu autorizar temporariamente o uso emergencial de vacinas contra a Covid-19, que ainda estão em fase de teses. De acordo com as informações do G1, apesar da autorização, Alessandra Bastos Soares, diretora da Anvisa, disse que a agência ainda não recebeu nenhum pedido de uso emergencial ou solicitação para registro de vacinas.

A diretora ainda reforçou que esse pedido deve ser feito pela empresa. “Qualquer autorização concedida pela Anvisa, qualquer anuência, só será feita diante de um pleito. A vacina só terá autorização de uso emergencial e experimental se houver o pleito realizado por alguma empresa”, disse Alessandra.
Além disso, a A Anvisa ainda ressaltou que poderá modificar, suspender ou cancelar a autorização temporária a qualquer momento, com base em elementos técnicos e científicos.
No momento, no Brasil existem quatro vacinas na fase final de testagem, desenvolvidas pelas seguintes empresas: AstraZeneca, em parceria com a Universidade de Oxford; Pfizer, em parceria com a BioNTech; Johnson & Johnson, por meio da subsidiária Janssen, e a Coronavac, do laboratório Sinovac.
As etapas de produção de uma vacina envolvem 3 fases:
Fase 1: avaliação preliminar com poucos voluntários adultos monitorados de perto;
Fase 2: testes em centenas de participantes que indicam informações sobre doses e horários que serão usados na fase 3. Pacientes são escolhidos de forma aleatória e são bem controlados;
Fase 3: teste em larga escala (com milhares de indivíduos) que precisa fornecer uma avaliação definitiva da eficácia/segurança e prever eventos divergentes.
Leia também

Família
Bruna Biancardi mostra a cor dos olhos de Mavie em novo foto: "Igual ao pai"

Bebês
Nomes japoneses femininos: 304 opções lindas para você conhecer

Bebês
180 nomes femininos diferentes: ideias de A a Z para você chamar a sua filha

Família
Homem que teve pênis amputado pela ex-esposa reata com ela e se declara: 'Te amo além da tragédia'
Gravidez
Sintomas de gravidez: nos primeiros dias, que ninguém sabe, de menino e menina e muito mais

Bebês
Nomes americanos femininos: mais de 1000 opções diferentes para você se inspirar

Bebês
210 nomes masculinos para bebês: ideias fortes (e lindas!) para você chamar o seu filho

Família
Bartolinite: o que é a bola inchada na vagina e como tratar a infecção